Hiểu được định nghĩa nguyên tố hoá học là gì tương đương với việc bạn đã nắm giữ chìa khoá mở cánh cửa đầu tiên để khám phá môn hoá này. Nguyên tố hoá học không chỉ là dấu hiệu trên bảng tuần hoàn mà chúng còn là yếu tố quyết định của mọi chất.
Nguyên tố hoá học nắm giữ vai trò quan trọng trong việc hình thành nên các phản ứng hoá học, sự hiểu biết về vật lý, sinh học và nhiều lĩnh vực khác. Nhằm giúp bạn có thêm nhiều kiến thức hữu ích hơn xoay quanh nội dung nguyên tố hoá học, chúng tôi sẽ cùng bạn tìm hiểu nội dung chi tiết hơn nhé!
Nguyên tố hoá học là gì?
Định nghĩa
“Nguyên tố hóa học là tập hợp các nguyên tử cùng loại, có cùng số proton trong hạt nhân. Mỗi nguyên tố được xác định theo số proton trong hạt nhân nguyên tử”.
Khi chúng ta thêm nhiều proton vào một nguyên tử thì có thể dẫn đến việc tạo ra một nguyên tố hoàn toàn mới. Proton. Đây là một trong những thành phần cơ bản của nguyên tử, đóng vai trò quan trọng trong xác định tính chất và đặc điểm của nguyên tố đó. Khi số proton trong hạt nhân tăng lên, nguyên tử trở nên khác biệt. Nó tạo ra một nguyên tố mới có tính chất và hành vi riêng biệt.
Bài viết này được đăng lần đầu tiên trên website Bảng tuần hoàn hóa học. Mọi trang web khác sử dụng nội dung này đều là copy!
Một điều quan trọng cần lưu ý là các nguyên tử cùng thuộc về một nguyên tố sẽ có cùng số hiệu nguyên tử, được ký hiệu là Z. Số hiệu nguyên tử là chỉ số đặc trưng cho mỗi nguyên tố, xác định số proton trong hạt nhân của nguyên tử đó.
Do đó, dù có sự biến đổi về cấu trúc nguyên tử, các nguyên tử của cùng một nguyên tố vẫn giữ nguyên số hiệu nguyên tử không đổi.
Phân loại các nguyên tố hoá học
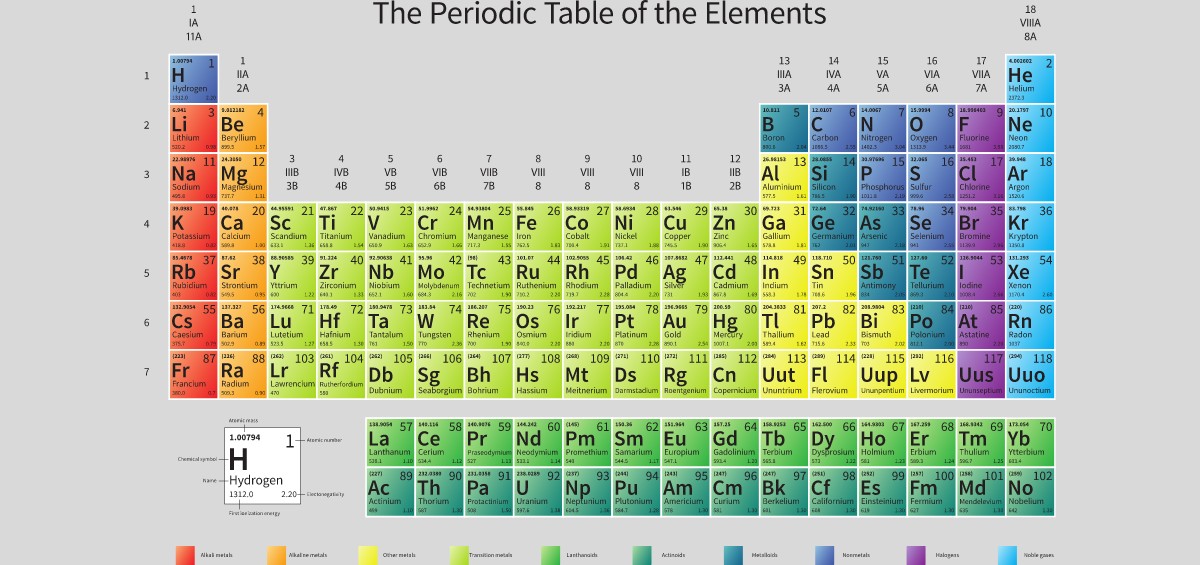
Bảng tuần hoàn hóa học có tổng cộng 118 nguyên tố hoá học. Nó được xem là bản đồ hữu ích giúp chúng ta hiểu về sự đa dạng của thế giới nguyên tố. Các nguyên tố được sắp xếp theo số proton trong hạt nhân, từ thấp đến cao.
Nhìn chung, chúng ta có thể phân loại các nguyên tố thành nhóm kim loại, nhóm phi kim, nhóm khí hiếm. Mỗi nhóm mang đặc điểm riêng, đóng góp vào sự hiểu biết sâu rộng về tính chất và ứng dụng của từng nguyên tố.
Kim loại
Nguyên tố kim loại, thường tồn tại dưới dạng đơn chất, thường là thể rắn trong điều kiện thông thường. Chúng cũng có một số ngoại lệ như thuỷ ngân, xeri và gali ở dạng lỏng. Trên bảng tuần hoàn hóa học, chúng ta đã xác định 81 nguyên tố kim loại, mỗi nguyên tố đóng góp vào sự đa dạng và quan trọng của hóa học.

Oxit của nguyên tố kim loại thường là oxit bazơ hoặc oxit lưỡng tính. Tong một số trường hợp với mức oxi hoá cao, oxit của chúng có thể là oxit axit. Các nguyên tố kim loại thường có từ 1 đến 3 electron ở lớp ngoài cùng.
Phi kim
Nguyên tố phi kim thường xuất hiện ở dạng đơn chất và là khí trong điều kiện thường. Trên bảng tuần hoàn, chúng ta đã xác định 16 nguyên tố phi kim, mỗi nguyên tố mang theo đặc tính riêng biệt.
Oxit của nguyên tố phi kim thường là oxi axit hoặc oxit trung tính. Số electron ở lớp ngoài cùng của chúng thường là từ 4 đến 7, trừ các khí hiếm có 8 electron ở lớp ngoài cùng.
Khí hiếm
Nguyên tố khí hiếm là nhóm đặc biệt. Nhóm nguyên tố hoá học này tồn tại dưới dạng đơn chất và là chất bán dẫn, thường kết hợp cả tính chất của kim loại và phi kim. Trong bảng tuần hoàn, có 5 nguyên tố á kim gồm Bo, Silic, Asen, Telu và Gemani.

Oxit của chúng thường là oxit lưỡng tính, tạo nên một nhóm nguyên tố đặc trưng trong thế giới hóa học.
Các tính chất của một nguyên tố hoá học
Nguyên tố hoá học có tính chất vật lý, tính chất hoá học và tính chất đặc biệt. Dưới đây chúng tôi sẽ đi vào nội dung chi tiết:
Tính chất vật lý
Tính chất vật lý của một nguyên tố hoá học là những đặc điểm mà chúng ta có thể quan sát và đo lường trực tiếp.
Khối lượng nguyên tử (Atomic Mass): Đây là cân nặng trung bình của một nguyên tử của nguyên tố.
Ví dụ: Nếu chúng ta nghĩ về nguyên tử như viên bi, khối lượng nguyên tử là cân nặng của viên bi đó.
Bán kính nguyên tử (Atomic Radius): Bán kính nguyên tử là khoảng cách từ trung tâm của hạt nhân đến lớp ngoài cùng của electron. Nguyên tử lớn có bán kính lớn, như những quả bóng bay to.
Nhiệt độ nóng chảy và nhiệt độ sôi: Khi nhiệt độ tăng lên, một nguyên tố có thể chuyển từ trạng thái rắn sang lỏng (nóng chảy) và từ lỏng sang hơi (sôi).

Tính chất hoá học
Tính chất hoá học của nguyên tố hoá học liên quan đến cách một nguyên tố tương tác và kết hợp với các nguyên tố khác để tạo ra các chất mới.
Electron ở ngoài cùng: Số electron ở lớp năng lượng cuối cùng quyết định tính chất hóa học. Nó giống như số bạn cuối cùng trong số điện thoại, đó là người bạn thường xuyên liên lạc.
Năng lượng ion hoá: Đây là năng lượng cần thiết để loại bỏ một electron từ nguyên tử và tạo thành ion dương. Năng lượng ion hoá càng cao, càng khó để tách electron ra khỏi nguyên tử.
Ái lực electron: Là khả năng của một nguyên tố “muốn” nhận thêm electron để trở thành ion âm. Nếu nguyên tố “muốn” nhiều electron, ái lực electron sẽ cao.
Tính chất đặc biệt
Bên cạnh tính chất vật lý và tính chất hoá học thì nguyên tố hoá học cũng có những tính chất đặc biệt khác. Những tính chất đặc biệt là những đặc điểm nổi bật và đặc trưng của mỗi nguyên tố.
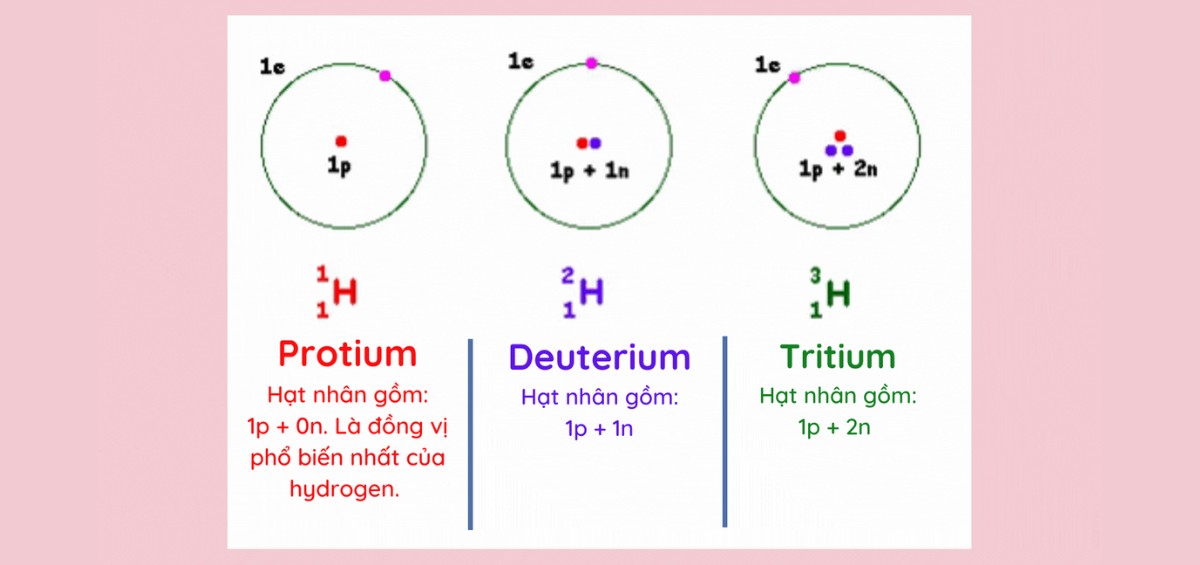
Đồng vị: Một nguyên tố có thể có nhiều phiên bản khác nhau với số lượng hạt nhân giống nhau nhưng số lượng electron khác nhau.
Hóa trị: Hóa trị biểu thị khả năng của nguyên tố “tích điện” bao nhiêu, tức là nhận bao nhiêu electron hoặc để bao nhiêu electron đi.
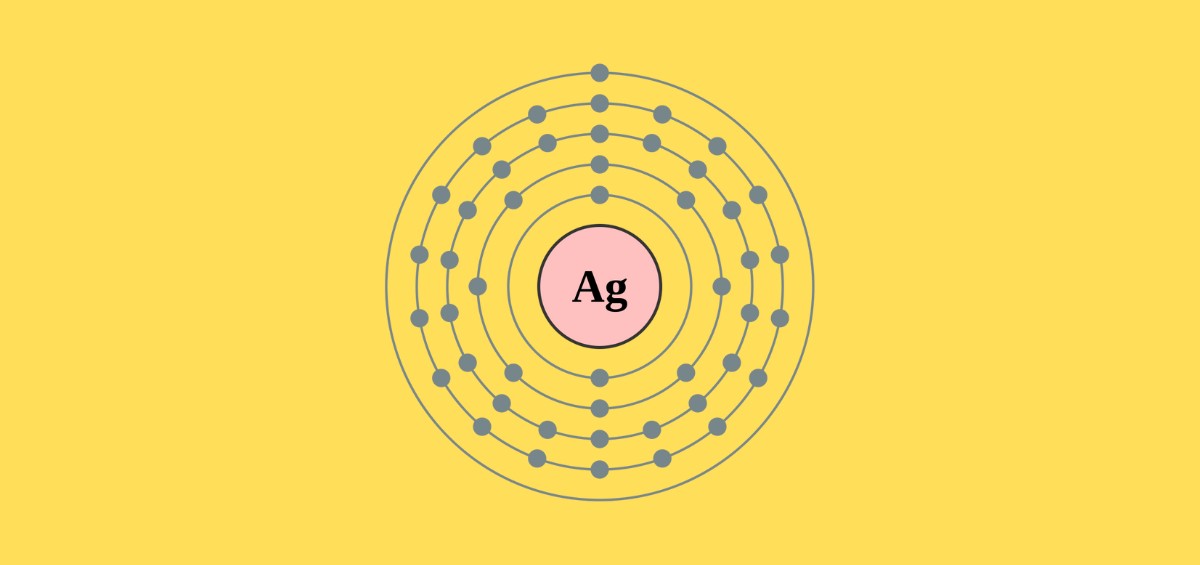
Cấu trúc electron: Là cách electron phân bố xung quanh hạt nhân, giống như cách chúng ta sắp xếp đồ trong tủ.
Những tính chất này cùng nhau tạo nên bảng tuần hoàn. Nó giúp chúng ta hiểu rõ về thế giới của các nguyên tố hóa học.
Trên đây, chúng tôi vừa giới thiệu đến bạn định nghĩa nguyên tố hoá học là gì. Theo kèm đó là kiến thức bổ sung xoay quanh định nghĩa, phân loại cũng như tính chất khác. Hy vọng, với những thông tin trên, nó sẽ là tiền đề hữu ích để bạn bắt đầu khám phá hoá học bằng một niềm yêu thích, say mê và phấn khởi.