Để có thể lập được công thức hoá học của một hợp chất nào đó, việc biết được hoá trị nguyên tố hoá học là điều vô cùng quan trọng. Con số hoá trị có thể giúp thể hiện khả năng liên kết các nguyên tử với nhau. Để giúp bạn đi sâu hiểu hoá trị là gì, cùng khám phá trong bài viết ngay sau đây nhé!
Hoá trị là gì?
Theo nội dung của sách giáo khoa hoá học lớp 8 do nhà xuất bản giáo dục Việt Nam viết thì hoá trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác. Hóa trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị và hóa trị của O là hai đơn vị.
Bài viết này được đăng lần đầu tiên trên website Bảng tuần hoàn hóa học. Mọi trang web khác sử dụng nội dung này đều là copy!
Ví dụ hoá trị của nguyên tố được thể hiện như sau:
- Trong NH3 thì nito có hoá trị III.
- Trong CaO thì canxi có hoá trị II.
- Trong FeCle2 thì sắt có hoá trị II.
- Trong FeCle3 thì sắt có hoá trị III.
Bảng hoá trị các nguyên tố hoá học
Biết được bảng hoá trị của các nguyên tố hoá học giúp bạn nắm vững nội dung hoá trị là gì. Đồng thời, khi vận dụng các bài học liên quan đến hoá trị thì bạn có thể chủ động lý giải một cách dễ dàng. Đừng quên sử dụng bảng tuần hoàn hoá học hỗ trợ bạn nữa nhé!
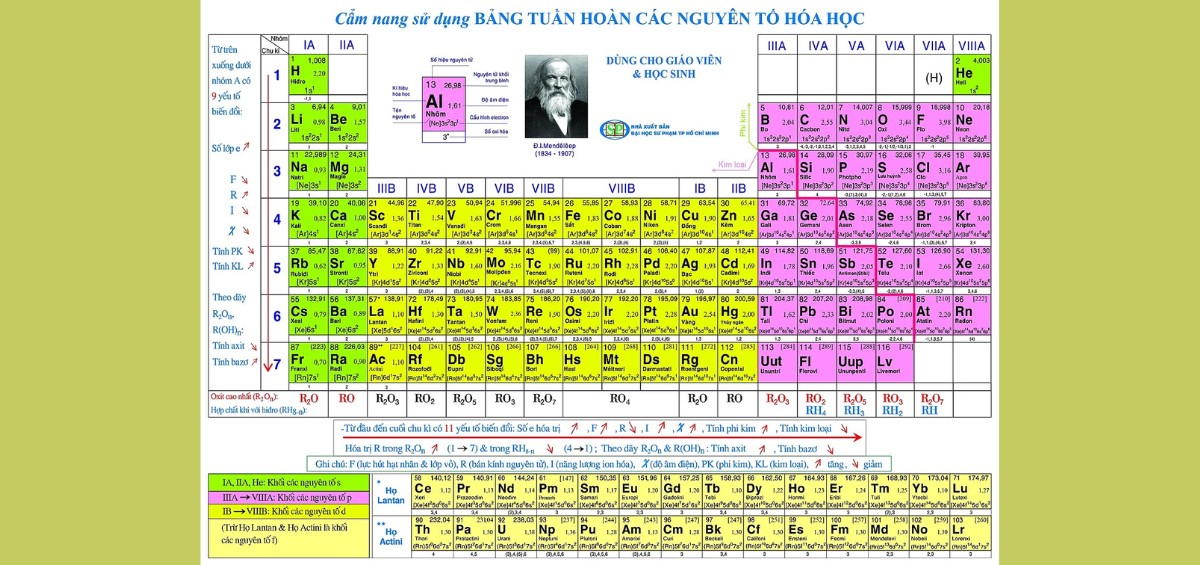
Bảng hoá trị các nguyên tố phổ biến
Dưới đây là bảng hoá trị hoá học các nguyên tố phổ biến nhất:
[table id=2 /]Bảng hoá trị một số nhóm nguyên tử phổ biến
Bên cạnh bảng hoá trị các nguyên tố thì bạn cũng cần tham khảo thêm nội dung bảng hoá trị một số nhóm nguyên tử phổ biến như sau:
[table id=3 /]Cách xác định hoá trị của một nguyên tố
Sau khi biết hoá trị là gì, để xác định được hoá trị của một nguyên tố thì bạn cần làm theo các bước sau:
Về quy ước: Để giúp cho việc xác định hoá trị của một nguyên tố hoá học đơn giản thì người ta sẽ gán hoá trị của H là I và O là II.
Xem xét số lượng liên kết với H: Số lượng liên kết với H sẽ giúp cho biết hoá trị của chính nguyên tố đó. Ví dụ: Trong hợp chất HCl thì Cl liên kết với H. Vì vậy Cl có hoá trị là i.
Xem xét số lượng liên kết với O: Số lượng liên kết với O (nếu có) sẽ được cộng vào hoá trị hiện tại của nguyên tố đó. Ví dụ: Trong hợp chất SO2 thì S liên kết với 2 O và O có hoá trị II nên hoá trị của S sẽ là IV.
Xem xét hoá trị của các nhóm nguyên tố: Ở một số trường hợp thì các nhóm nguyên tử có thể ảnh hưởng đến hoá trị của nguyên tố đó trong hợp chất. Ví dụ: Trong hợp chất H2SO4 thì nhóm SO4 có hai liên kết với H nên hoá trị của nhóm SO4 là II.
Quy tắc hoá trị cơ bản nhất
Quy tắc hoá trị được thể hiện nội dung như sau: Tích của chỉ số với hóa trị của nguyên tố này, bằng tích của chỉ số với hóa trị của nguyên tố kia.
Ví dụ: Một hợp chất Kali Clorua (KCl).
Áp dụng quy tắc hoá trị ta có:
Hoá trị của K thường là I vì nó ở cột IA và hoá trị của Cl thường là I vì nó ở cột VIIA.
Theo quy tắc hoá trị ta có: X * hoá trị của K = y * hoá trị của Cl. Ở trường hợp này, x = y – 1 vì hoá trị của nguyên tố hoá học K và Cl đều là 1.
Vì vậy, công thức chính xác cho KCl với hoá trị của K là I và hoá trị của Cl cũng là I. Với ví dụ này, bạn có thể thấy rằng thông qua quy tắc hoá trị, bạn có thể xác định được hoá trị của nguyên tố trong một hợp chất đơn giản.

Bài ca hoá trị dễ nhớ nhất
Việc ghi nhớ hoá trị trong một hoá là một trong những trở ngại khiến nhiều người e dè. Dưới đây là một số bài ca hoá trị đơn giản, dễ nhớ nhất.
Bài số 1
“Kali (K), Iot (I), Hidrô (H)
Natri (Na) với Bạc (Ag), Clo (Cl) một loài
Là hoá trị I hỡi ai
Nhớ ghi cho kỹ khỏi hoài phân vân
Magiê (Mg), Kẽm (Zn) với Thuỷ Ngân (Hg)
Oxi (O), Đồng (Cu), Thiếc(Sn) thêm phần
Bari (Ba) Cuối cùng thêm chú Canxi (Ca).”
Bài số 2
“Hoá trị II nhớ có gì khó khăn
Bác Nhôm (Al) hoá trị III lần
In sâu trí nhớ khi cần có ngay
Cacbon (C), Silic (Si) này đây
Có hoá trị IV không ngày nào quên
Sắt (Fe) kia lắm lúc hay phiền
II, III lên xuống nhớ liền ngay thôi
Nitơ (N) rắc rối nhất đời
I, II, III, IV khi thời lên V
Lưu huỳnh (S) lắm lúc chơi khăm
Xuống II lên VI khi nằm thứ IV
Phot pho (P) nói đến không dư
Có ai hỏi đến thì ừ rằng V
Em ơi, cố gắng học chăm
Bài ca hoá trị suốt năm cần dùng.”
Bài số 3
“Ca là chú Can xi
Ba là cậu Bari họ hàng
Au tên gọi là Vàng
Ag là Bạc cùng làng với nhau
Viết Đồng C trước u sau
Pb mà đứng cùng nhau là Chì
Al đấy tên gì?
Gọi Nhôm bác sẽ cười khì mà xem
Cacbon vốn tính nhọ nhem
Kí hiệu C đó bạn đem nhóm lò
Oxy O đấy lò dò
Gặp nhau hai bạn cùng hò cháy to
Cl là chú Clo
Lưu huỳnh em nhớ viết cho S (ét sờ).
Zn là Kẽm khó gì.”

Một số bài tập trắc nghiệm hoá học về hoá trị
Câu 1
Câu hỏi: Hóa trị của một nguyên tố (hay nhóm nguyên tử) là con số biểu thị
A. số nguyên tử của nguyên tố (hay số nhóm nguyên tử) đó trong hợp chất.
B. khả năng liên kết của nguyên tử (hay nhóm nguyên tử).
C. khối lượng của nguyên tố (hay nhóm nguyên tử) đó trong hợp chất.
D. phần trăm khối lượng của nguyên tố (hay nhóm nguyên tử) đó trong hợp chất.
Đáp án: B. khả năng liên kết của nguyên tử (hay nhóm nguyên tử).
Câu 2
Câu hỏi: Cho biết sơ đồ công thức của hợp chất giữa nguyên tố X với H và O như sau: H – X – H, X = O. Quy ước mỗi vạch ngang giữa hai kí hiệu biểu thị một hóa trị của mỗi bên nguyên tử. Hóa trị của X là
A. I.
B. III.
C. II.
D. IV.
Đáp án: C. II.

Câu 3
Câu hỏi: Hóa trị của C trong hợp chất CH4 là
A. II.
B. III.
C. IV.
D. VI.
Đáp án: C. IV.
Câu 4
Câu hỏi: Phân tử của một hợp chất tạo bởi Na hóa trị I và nhóm (OH) hóa trị I. Tổng số nguyên tử của các nguyên tố trong hợp chất là
A. 1.
B. 3.
C. 4.
D. 2.
Đáp án: B. 3.
Câu 5
Câu hỏi: Khi phân tích hợp chất (X) chứa 27,273% cacbon và còn lại là oxi. Hóa trị của cacbon trong hợp chất trên là bao nhiêu?
A. I
B. II
C. III
D. IV
Đáp án: D. IV
Chúng tôi hy vọng rằng bạn đã hiểu được hoá trị là gì. Thông qua hoá trị, bạn có thể biết được cách xác định hoá trị và quy tắc hoá trị chính xác. Đặc biệt là áp dụng kiến thức vào các bài học hoá học, bài tập một cách thành công.